Bioquímica: Você realmente entende o que acontece dentro das células?
Muito além de reações e moléculas, existe um universo complexo de processos que sustentam a vida em cada organismo. Mas conhecer termos não é o mesmo que compreender como tudo funciona. Descubra o quanto você realmente sabe sobre bioquímica.
Por que testar seus conhecimentos?
Testar seus conhecimentos melhora a memória, o raciocínio rápido e a capacidade de associação, além de ser uma forma divertida de aprender enquanto compete com outras pessoas.
A Ciência dos Processos Moleculares da Vida
A bioquímica é a ciência que estuda as reações químicas e processos moleculares que ocorrem nos organismos vivos. Essa área interdisciplinar combina princípios da química e da biologia para compreender o funcionamento das células, incluindo a estrutura e função de biomoléculas como proteínas, carboidratos, lipídios e ácidos nucleicos.
A bioquímica tem aplicações fundamentais na medicina, biotecnologia, nutrição e farmacologia, permitindo avanços na compreensão de doenças, no desenvolvimento de medicamentos e na engenharia de biomoléculas para diversos setores industriais. Técnicas como a engenharia genética e a biologia molecular impulsionam pesquisas sobre metabolismo, sinalização celular e regulação gênica.
Além disso, a bioquímica é essencial para áreas emergentes, como a bioquímica clínica e a biotecnologia industrial, que buscam soluções inovadoras para a saúde humana e sustentabilidade. Seu impacto se estende desde a descoberta de novos tratamentos até a produção de alimentos e biocombustíveis, tornando-se uma ciência indispensável para o avanço tecnológico e científico.
A Base da Vida e o Papel das Proteínas
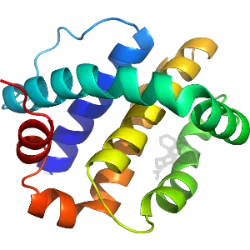
As biomoléculas são fundamentais para a vida, e entre elas, as proteínas desempenham papéis essenciais na estrutura e funcionamento dos organismos. Elas são compostas por aminoácidos e organizadas em quatro níveis estruturais: a estrutura primária corresponde à sequência linear de aminoácidos; a secundária, às dobras formadas por ligações de hidrogênio, como as hélices alfa e folhas beta; a terciária define a forma tridimensional da proteína; e a quaternária surge quando duas ou mais cadeias polipeptídicas se unem.
Além de estruturar tecidos, as proteínas atuam como enzimas, catalisadores biológicos que aceleram reações químicas essenciais, como a digestão e a produção de energia. A catálise enzimática ocorre por meio da redução da energia de ativação, tornando os processos celulares mais eficientes.
Pesquisas na bioquímica têm revelado novas funções das proteínas e suas aplicações na medicina e na biotecnologia. O estudo dessas biomoléculas é crucial para avanços em tratamentos de doenças e na engenharia de novos fármacos.
Descubra mais curiosidades sobre Bioquímica
A Principal Fonte de Energia para a Vida
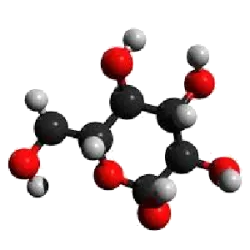
Os carboidratos são biomoléculas essenciais para os organismos vivos, desempenhando papéis fundamentais na produção de energia e na estrutura celular. Eles são classificados em três grupos principais: monossacarídeos, como a glicose e a frutose, que são açúcares simples e rapidamente absorvidos; dissacarídeos, como a sacarose e a lactose, compostos por dois monossacarídeos unidos; e polissacarídeos, como o amido e o glicogênio, que funcionam como reservas energéticas em plantas e animais.
Além de fornecerem energia, os carboidratos também possuem função estrutural. A celulose, presente na parede celular das plantas, garante rigidez e sustentação, enquanto a quitina fortalece exoesqueletos de insetos e crustáceos.
Na saúde humana, a ingestão equilibrada de carboidratos é crucial, pois o excesso pode levar a doenças metabólicas, como diabetes. Estudos avançam na compreensão dessas biomoléculas e seu impacto na nutrição e biotecnologia.
Essenciais para Energia e Estrutura Celular

Os lipídios são biomoléculas fundamentais para os organismos vivos, desempenhando papéis cruciais no armazenamento de energia e na estrutura das células. Entre os principais tipos, estão os ácidos graxos, que servem como fonte primária de energia; os triglicerídeos, armazenados no tecido adiposo para reserva energética; os fosfolipídios, que compõem a membrana celular e garantem sua fluidez e proteção; e os esteróis, como o colesterol, essencial para a síntese de hormônios e estabilização das membranas.
Além de fornecer energia de longa duração, os lipídios atuam na isolação térmica e proteção dos órgãos. No metabolismo, são quebrados por enzimas e transportados pelo sangue para serem usados como combustível celular. Apesar de sua importância, o excesso de lipídios pode estar associado a doenças cardiovasculares.
Estudos avançam no entendimento dessas biomoléculas para desenvolver novos tratamentos para obesidade e distúrbios metabólicos, destacando a importância do equilíbrio na dieta.
Os ácidos nucleicos, DNA e RNA
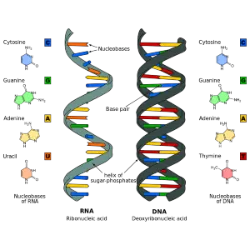
Os ácidos nucleicos, DNA e RNA, são biomoléculas essenciais que armazenam e transmitem a informação genética dos seres vivos. O DNA (ácido desoxirribonucleico) contém as instruções para a formação e funcionamento das células, sendo responsável pela hereditariedade. Já o RNA (ácido ribonucleico) desempenha papel crucial na síntese de proteínas, traduzindo o código genético em moléculas funcionais.
O processo inicia-se com a transcrição, onde o DNA é convertido em RNA mensageiro (mRNA). Em seguida, ocorre a tradução, na qual ribossomos e RNA transportador (tRNA) organizam aminoácidos para formar proteínas, essenciais para as funções celulares.
Além da síntese proteica, os ácidos nucleicos regulam a expressão gênica, controlando quais genes são ativados ou silenciados. Pesquisas avançadas em biotecnologia e terapia genética exploram essas biomoléculas para tratar doenças hereditárias e desenvolver novas terapias médicas, reforçando seu papel fundamental na ciência e na medicina.
Metabolismo: O Equilíbrio
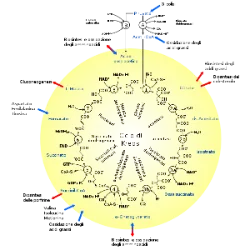
O metabolismo é um conjunto de reações químicas essenciais para a manutenção da vida, dividido em dois processos fundamentais: catabolismo e anabolismo. O catabolismo envolve a quebra de moléculas complexas, como carboidratos e lipídios, liberando energia em reações exergônicas – aquelas que produzem ATP, combustível celular. Exemplos incluem a glicólise e a respiração celular.
Por outro lado, o anabolismo é responsável pela construção de moléculas, como proteínas e DNA, consumindo energia em reações endergônicas. Esse processo é essencial para o crescimento celular, reparação de tecidos e armazenamento de energia, sendo impulsionado pelo ATP gerado no catabolismo.
O equilíbrio entre essas vias metabólicas garante o funcionamento do organismo. Estudos em bioenergética buscam otimizar esse processo para tratar doenças metabólicas e desenvolver terapias inovadoras, reforçando a importância dessas reações para a saúde e a ciência.
Os Caminhos do Metabolismo Celular
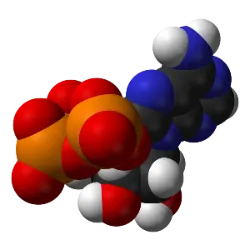
A produção de energia nas células depende de três processos fundamentais: glicólise, Ciclo de Krebs e Cadeia Transportadora de Elétrons. Esses mecanismos garantem a conversão de nutrientes em ATP, a principal fonte de energia celular.
A glicólise, primeira etapa, ocorre no citoplasma e quebra uma molécula de glicose em duas de piruvato, gerando ATP e NADH. Se houver oxigênio disponível, o piruvato segue para a mitocôndria, onde ocorre o Ciclo de Krebs. Nessa fase, moléculas de acetil-CoA são processadas, liberando CO₂ e produzindo mais NADH e FADH₂, transportadores de elétrons.
A última etapa é a Cadeia Transportadora de Elétrons, localizada na membrana mitocondrial. Nela, os elétrons passam por proteínas especializadas, gerando um gradiente de prótons que impulsiona a síntese de ATP. Esse processo finaliza a respiração celular e garante a maior produção energética do organismo.
HOME